نوروسافاری | مطالعه ی بالینی انجام شده با سرمایه گذاری انستیتو ملی سلامت (NIH)، از ارتباط بین میکروب های شکمی و سیستم ایمنی بدن با یک اختلال ژنتیکی خبر داد که میتواند باعث بروز سکته مغزی و تشنج شود.
به گزارش نوروسافاری به نقل از سایت خبری انستیتو ملی اختلالات عصبی و سکته (NINDS)، مطالعه ی انجام شده بر روی موش و انسان، نشان میدهد که باکتریهای موجود در شکم میتواند ساختار عروق خونی مغز را تحت تاثیر قرار داده و ممکن است سبب بروز ناهنجاری های ساختاری ای شود که باعث بروز سکته مغزی یا تشنج میشوند.
این پژوهش که در ژورنال Nature به چاپ رسیده است به مجموعه ی تحقیقات نوظهوری پیوسته است که بیماری های سیستم عصبی را به میکروب های روده مرتبط دانسته اند. این مطالعه با سرمایه گذاری انستیتو ملی اختلالات عصبی و سکته (NINDS) به عنوانی بخشی از NIH انجام شده است.
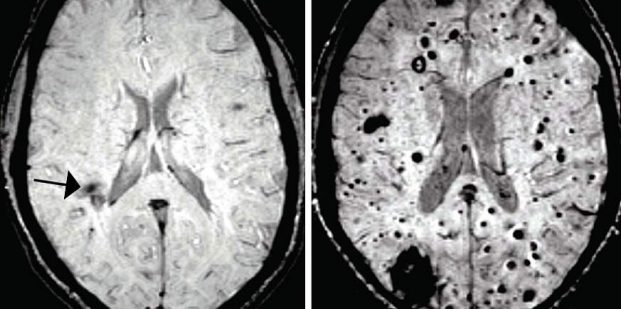
ناهنجاری های مغزی کاورنوس یا غار مانند (CCMs) دسته هایی از عروق خونی منبسط شده با دیواره های نازک شده هستند که میتوانند در هنگام نشت خون به بافت مغزی اطراف، باعث تشنج یا سکته شوند. تیمی از دانشمندان در دانشگاه پنسیلوانیا مکانیزم هایی را مورد بررسی قرار دادند که باعث تولید ضایعه های CCM در مغز موش هایِ مهندسیِ ژنتیک شده، میشوند؛ و سپس ارتباط غیر منتظره ای آن را با یک باکتری موجود در شکم پیدا کردند. زمانی که باکتری از بین رفت، تعداد ضایعات مذکور به طور چشم گیری کاهش یافت.
دکتر جیم آی. کوئینگ سرپرست برنامه در NINDS گفت: ” این مطالعه بسیار هیجان انگیز است زیرا نشان میدهد تغییرات درون بدن میتوانند روی میزان پیشروی بیماری هایی که بر اثر جهش های ژنتیکی ایجاد شده اند تاثیر بگذارند.”
محققان در حال مطالعه بر روی یک مدل موش بودند که پس از تزریق یک دارو (برای ایجاد شرایط حذف ژنی)، تعداد قابل توجهی ضایعات CCM در مغز آن شکل میگرفت. با این حال، وقتی این حیوان به محل آزمایشگاه دیگری منتقل شد، فرکانس شکل گیری ضایعه ها در مغز آن تقریبا به صفر رسید.
دکتر مارک ال. کان، استاد دانشکده پزشکی دانشگاه پنسیلوانیا و نویسنده ارشد این مطالعه گفت: ” این اتفاق مثل یک معما بود. به طور کاملا ناگهانی مغز مدل حیوانی (موش) قابل اعتماد ما، دیگر قادر نبود ضایعات CCM را، بر اساس انتظارات قبلی، تولید کند. جالب است که این متغیر بودن در شکل گیری ضایعه های CCM در مغز انسان نیز دیده میشود؛ به طوری که بیمارانی با جهش های ژنتیکی مشابه (یکسان) اغلب به طور چشم گیری دارای مسیرهای متفاوتی در پیشرفت بیماری هستند.”
در حین تحقیق در مورد این تغییر ناگهانی، آلن تانگ، دانشجوی تحصیلات تکمیلی آزمایشگاه دکتر کان، مشاهده کرد که در شکم تعداد اندکی از موش ها، که روند تشکیل ضایعات در آنها ادامه پیدا کرده بود، آبسه های باکتریایی ایجاد شده است. این عفونت احتمالا بر اثر تزریقات شکمی دارو در موش ها به وجود آمده بود. آبسه ها، باکتری های گرم-منفی را در خود جای داده بودند. زمانی که این عفونت باکتریایی، عمدا در موش های مدل CCM ایجاد شد، تقریبا در مغز نیمی از آنها، باعث شکل گیری ضایعات قابل توجهی شد.
آلن تانگ گفت: ” موش هایی که ضایعات CCM در مغز آنها ایجاد شده بود، در طحالشان نیز آبسه های باکتریایی وجود داشت که نشان دهنده ی ورود عفونت به جریان خون از محل اولیه ی آبسه ها بود. این پدیده نشان دهنده ی ارتباط بین گسترش نوع خاصی از باکتری در جریان خون با شکل گیری این ضایعه های عروق خونی در مغز است.”
حال سوال اینجا بود که حضور این باکتری ها در جریان خون، چگونه میتواند رفتار عروق خونی مغز را تحت تاثیر قرار دهد. باکتری گرم-منفی، مولکول هایی با نام (lipopolysaccharides (LPS تولید میکنند که پتانسیل بالایی در فعالسازی سیگنال های طبیعی سیستم ایمنی دارند. زمانی که به موش ها، فقط LPS تزریق شد، تعداد زیادی ضایعات CCM بزرگ در مغز آنها شکل گرفت؛ درست شبیه مواردی که در عفونت باکتریایی ایجاد شده بود. در مقابل، زمانی که گیرنده های LPS (با نام TLR4) به صورت ژنتیکی در موش ها حذف شدند، دیگر ضایعه ای در مغز آنها ایجاد نشد. محققین دریافتند که در انسان ها نیز، جهش های ژنتیکی ای که باعث افزایش بیان TLR4 میشوند، با افزایش ریسک شکل گیری CCMs در ارتباط هستند.
دکتر کان گفت: ” میدانیم که شکل گیری ضایعه ها میتواند در اثر حضور باکتری گرم-منفی در بدن و در جریان ارتباطات سیگنالی LPS رخ بدهد. سوال بعدی ما این بود که آیا میتوانیم با تغییر باکتری در درون بدن از تشکیل ضایعه ها جلوگیری کنیم.”
محققان، تغییرات باکتری های بدن (میکروبیوم) را با دو روش بررسی کردند. اول، موش های مدل CCM را در شرایط عادی یا شرایط بدون میکروب پرورش دادند. دوم، به این موش ها آنتی بیوتیک داده شد که میکروبیوم آنها مجددا تنظیم شود. در هر دو حالت، هم تزریق آنتی بیوتیک و هم شرایط بدون میکروب، تعداد ضایعه ها به طور قابل ملاحظه ای کاهش یافت که نشان میدهد دو عامل کمیت و کیفیت میکروبیوم شکم میتواند در شکل گیری CCM ها تاثیرگذار باشد. در نهایت، دارویی که گیرنده های TLR4 را مسدود میکند، به طور چشم گیری، تشکیل ضایعات را کاهش داد. این دارو برای درمان عفونت منتشر خونی (سپسیس) مورد تست بالینی قرار گرفته است و اکنون نیز پتانسیل اثر درمانی آن در CCMs مشاهده شده است. با این حال تحقیقات زیادی در این زمینه باید انجام شود.
دکتر کوئینگ گفت: ” نتایج حاکی از آن است که میتوان یافته ها را بر روی جمعیت بیماران (انسان) نیز تست کرد. دارویی که گیرنده های TLR4 را مسدود میکند، پیش از این برای درمان بیماری دیگری بر روی انسان تست شده است، و ممکن است پتانسیل درمانی برای درمان CCMs داشته باشد و البته تحقیقات زیادی هنوز در این زمینه باید انجام شود.”
دکتر کان و همکارانش قصد دارند تا به مطالعه بر روی ارتباط بین میکروبیوم و تشکیل ضایعه ها CCM ادامه بدهند زیرا به بیماری انسانی مرتبط است. علیرغم شناسایی جهش های ژنی مسئول تشکیل ضایعه های CCM، اندازه و تعداد این ضایعه ها در بین بیمارانی با جهش های ژنی یکسان، به طور گسترده ای متفاوت است. هدف بعدی این گروه بررسی این فرضیه است که تفاوت های موجود در میکروبیوم بیماران میتواند توضیحی برای متغیر بودن تعداد ضایعه ها باشد یا نه.
ترجمه : سید محمد رضا گواهی – وبسایت نوروسافاری
منبع گزارش خبری در سایت NINDS :
Researchers connect brain blood vessel lesions to intestinal bacteria
مرجع مقاله پژوهشی در ژورنال Nature :
Endothelial TLR4 and the microbiome drive cerebral cavernous malformations
 نوروسافاری | دانش مغز و علوم اعصاب دانش مغز و علوم اعصاب. در این وبسایت خلاصه ای از مهمترین تحقیقات همه رشته های علوم اعصاب و مغز را می توانید به زبان ساده بخوانید. تلاش ما جهت هم افزایی بین رشته ای جهت پیشرفت بیشتر این علم است.
نوروسافاری | دانش مغز و علوم اعصاب دانش مغز و علوم اعصاب. در این وبسایت خلاصه ای از مهمترین تحقیقات همه رشته های علوم اعصاب و مغز را می توانید به زبان ساده بخوانید. تلاش ما جهت هم افزایی بین رشته ای جهت پیشرفت بیشتر این علم است.