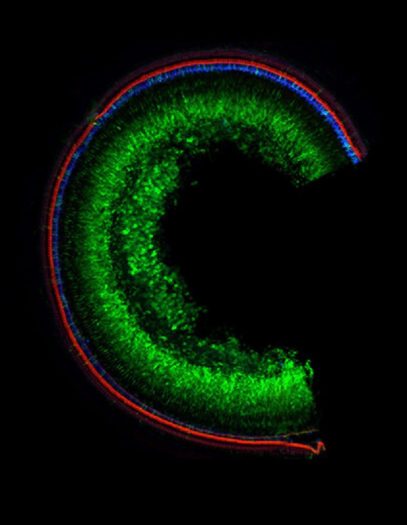
نوروسافاری | تصویر میکروسکوپ لیزری کانفوکال از حلزون موش، اندام شنوایی گوش داخلی. جسم سلولیهای حسی به رنگ آبی، اندامکهای حسی به رنگ قرمز و سلولهای دارای ژن Tmc1 ترمیم شده به رنگ سبز دیده می شوند.
هنگامی که وی هسی (آریل) ایه دانشجوی جوان کارشناسی بود، یکی از دوستان نزدیک او در عرض یک ماه از شنوایی طبیعی به سمت ناشنوایی کامل پیش رفت. او ۲۹ سال سن داشت. هیچ کس نمی دانست چرا شنوایی خود را از دست داده است. پزشکان هنوز نمی دانند. این مساله برای دوستش ناامید کننده و ترسناک بود، ایه، که ماه گذشته با مدرک دکترای شیمی خود از دانشگاه هاروارد فارغ التحصیل شد. مطالعات تکمیلی خود را به حل برخی از رازهای ژنتیکی بسیار در زمینه از دست دادن شنوایی اختصاص داد.
در ایالات متحده، از هر ۸ نفر یک نفر در سن ۱۲ سال یا بالاتر، در هر دو گوش دچار کم شنوایی هستند. در حالی که فناوری هایی مانند سمعک و کاشت حلزون می توانند صدا را تقویت کنند، اما نمی توانند مشکل را حل کنند. اما ویرایش ژن می تواند- ناهنجاری های ژنتیکی در نیمی از همه موارد نقش دارند. دو سال پیش، ایه و دیوید آر. لیو، توماس دادلی کابوت استاد علوم طبیعی و عضو انستیتوی واد و موسسه پزشکی هوارد هیوز، یک جهش غالب را ترمیم کردند و برای اولین بار مانع از دست دادن شنوایی در یک مدل موش شدند. لیو گفت:
بیشتر بیماریهای ژنتیکی ناشی از جهش های غالب نیستند، بلکه بیشتر در اثر بیماریهای مغلوب ایجاد میشوند.
اکنون، لیو، ایه و محققان دانشگاه هاروارد، انستیتوی Broad و موسسه پزشکی هوارد هیوز به اولین دستاورد دیگری رسیدند: آنها شنوایی نسبی را به موش هایی که دارای جهش مغلوب در ژن TMC1 هستند و باعث ناشنوایی کامل می شود، بازگرداندند، اولین نمونه موفق ویرایش ژنوم برای رفع یک جهش مغلوب منجر به یک بیماری است.
جهش های منجر به بیماری در ژن غالب
جهش های منجر به بیماری در ژن غالب، به این معنی است که اگر در مواردی فقط یکی از دو نسخه از ژن تغییر یابد و جهش یابد، از بعضی جهات حمله به آن راحت تر است. نسخه بد را حذف کنیم و نسخه دوم خوب نجات دهنده خواهد بود. لیو گفت:
اما در مورد بیماریهای مربوط به جهش در ژن های مغلوب، شما نمی توانید این کار را انجام دهید. طبق تعریف،در بیماریهای مربوط به آلل مغلوب به معنای این است که دو نسخه بد دارید. بنابراین، شما نمی توانید فقط یک نسخه بد را نابود کنید.
شما باید یکی یا هردو را اصلاح کنید.
حیوانات برای شنیدن به سلولهای مویی گوش داخلی تکیه دارند که تحت فشار امواج صوتی خم می شوند و پیام های الکتریکی را به مغز می فرستند. جهش مغلوب TMC1 که لیو و ایه امیدوار بودند که آن را اصلاح کنند باعث خراب شدن سریع آن سلولهای مویی شد و منجر به ناشنوایی عمیقی در ۴ هفتگی شد.
جفری هولت، استاد گوش و حلق و بینی و عصب شناسی در دانشکده پزشکی هاروارد و نویسنده مقاله، با موفقیت درمان ناشنوایی ناشی از TMC1 را با ژن درمانی انجام داد- آنها سلولهایی با نسخه های سالم ژن را در میان ناسالم ها برای مقابله با جهش ایجاد کننده بیماری فرستادند. اما اولگا شوبیناالینک، یکی از همکاران فوق دکتری در آزمایشگاه هولت، گفت که ژن درمانی ممکن است مدت محدودی داشته باشد.
به همین دلیل ما به تکنیکهای پیشرفته تری نظیر ویرایش ژن نیاز داریم که ممکن است برای تمام طول عمر پایدار باشد.
فناوری ویرایش پایه
لیو از فناوری ویرایش پایه خود برای اصلاح یک جهش ژنتیکی مغلوب استفاده کرد که می تواند منجر به از دست دادن کامل شنوایی در انسان شود.
ایه سالهایی را در ساخت ویرایشگر پایه ای صرف کرد که می تواند جهش ایجاد کننده بیماری را پیدا کرده و از بین ببرد و آن را با کد صحیح DNA جایگزین کند. اما حتی بعد از اینکه نتایج خوبی را در شرایط آزمایشگاهی به دست آورد، هنوز مشکلی وجود داشت: ویرایشگرهای پایه برای قرار گرفتن در حامل سنتی تحویل، ویروس مرتبط با آدنو یا AAV بسیار بزرگ بودند. برای حل این مشکل، تیم ویرایشگر پایه را به نصف تقسیم کردند و هر قطعه را با حامل ویروسی مخصوص خود ارسال کردند. در داخل بدن، دو ویروس برای یافتن هدف خود نیاز به آلوده کردن سلول های مشابه دارند جایی که در آن دو ویرایشگر پایه با هم قرار میگیرند و با کمک هم هدفشان را پیدا میکنند. با وجود ورود به هزارتوی، ویرایشگر ثابت کرد که کارآمد بوده و حداقل حذف ها یا درج های ژنتیکی ناخواسته را ایجاد میکند.
لیو گفت:
ما شاهد شواهد بسیار کمی از ویرایش خارج از هدف بودیم.
و ما متوجه شدیم که حیوانات ویرایش شده دارای مورفولوژی سلولهای مویی و انتقال سیگنال بسیار حفظ شده هستند، یعنی سلولهای مویی، سلولهای کلیدی که امواج صوتی را به سیگنالهای عصبی تبدیل می کنند، طبیعی تر به نظر می رسند و سالم تر رفتار می کنند.
پس از معالجه
پس از معالجه، ایه یک آزمایش غیررسمی انجام داد: او دستانش را بهم زد. موشی که قبلاً تمام توانایی شنوایی را از دست داده بود، از جا پرید و برای دیدن چرخید. آزمایشات رسمی نشان داد که ویرایشگر پایه کار می کند، حداقل تا حدی، ایه گفت:
در موش های معالجه شده شنوایی تا حدی بازگشته بود و می توانستند به صدای بلند و حتی برخی از صداهای متوسط پاسخ دهند.
البته قبل از استفاده از این درمان در انسان باید کارهای بیشتری انجام شود. سلولهای ویرایش نشده به مرگ خود ادامه دادند و باعث بازگشت ناشنوایی حتی بعد از بازگردانی عملکرد توسط ویرایشگر پایه در برخی سلولها شدند.
اما این مطالعه همچنین ثابت کرد که روش تحویل مخفی AAV مؤثر است. در حال حاضر، لیو از AAV برای مقابله با سایر بیماری های ژنتیکی، از جمله پروگریا، کم خونی سلول داسی و بیماری های استحاله ای حرکتی استفاده می کند. لیو گفت:
اکنون ما واقعا گرفتار بیماری های ژنتیکی معدودی هستیم، از جمله برخی از بیماریهای بارزی که رنج بسیاری را باعث شده اند و به صرف انرژی بسیار زیادی در جمعیت بیماران مشتاق و خانواده های بیماران، به انجام هر کاری برای یافتن روشی درمانی وا داشته است.
در مورد پروگریا، هیچ درمانی وجود ندارد. بهترین روشهای درمانی میانگین طول عمر کودک را از حدود ۱۴ تا ۱۴٫۵ سال افزایش می دهد.
برای ایه، ناشنوایی ژنتیکی هنوز هم هدف اصلی اوست، اما هنوز هیچ پاسخی برای درمان کم شنوایی دوستش ندارد. او گفت:
هنوز چیزهای زیادی برای کشف وجود دارد.
چیزهای ناشناخته بسیار است.
ترجمه: رویا ورمزیار- وبسایت نوروسافاری
لینک خبر:
لینک مقاله:
 نوروسافاری | دانش مغز و علوم اعصاب دانش مغز و علوم اعصاب. در این وبسایت خلاصه ای از مهمترین تحقیقات همه رشته های علوم اعصاب و مغز را می توانید به زبان ساده بخوانید. تلاش ما جهت هم افزایی بین رشته ای جهت پیشرفت بیشتر این علم است.
نوروسافاری | دانش مغز و علوم اعصاب دانش مغز و علوم اعصاب. در این وبسایت خلاصه ای از مهمترین تحقیقات همه رشته های علوم اعصاب و مغز را می توانید به زبان ساده بخوانید. تلاش ما جهت هم افزایی بین رشته ای جهت پیشرفت بیشتر این علم است.